
Международная группа биохимиков продемонстрировала, каким образом гетеротрофные организмы могут расти и получать энергию, не используя глюкозу и жиры. Два таких способа были известны и раньше (их эксплуатируют животные, а также бактерии, растения и грибы). Теперь ученые знают, как это удается архебактериям — это третий, альтернативный, способ. Цепочка химических реакций, которую изобрели археи, пригодна для условий высокой солености и высокого содержания азотистых веществ. Этот третий способ позволяет не только синтезировать нужные углеводы, но и поддерживать осмотический баланс в клетке. Гены ферментов, обслуживающих эту химическую цепочку, археи позаимствовали у бактерий путем горизонтального переноса.
Каждое живое существо потребляет пищу. Для всех без исключения она служит источником строительного материала, энергии, а также катализаторов химических реакций и буферных веществ внутренней среды. Энергия в клетках аэробных организмов получается в ходе реализации цикла трикарбоновых кислот, или цикла Кребса, названного по имени открывшего его ученого. Этот цикл составляет цепочка последовательных реакций, в которых пировиноградная кислота (продукт расщепления глюкозы) через ряд промежуточных реакций превращается в углекислый газ и воду; на каждой стадии этого цикла работает свой фермент. Цель этих преобразований — получить и запасти максимальное количество энергии. Строительный материал для вхождения в этот цикл — молекула ацетила, соединенная с коферментом А, или ацетил-КоА, и низкомолекулярный углевод оксалоацетат. Все позвоночные берут эти базовые низкомолекулярные углеводы, в том числе и ацетил-КоА, посредством расщепления глюкозы и жиров (см.: Метаболизм кетоновых тел). Синтезировать ацетил и оксалоацетат они не умеют.
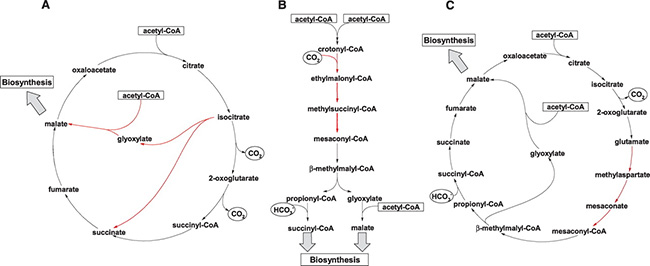
А вот растения, бактерии и грибы могут получать оксалоацетат и ацетил из другой цепочки реакций, сопряженной с циклом Кребса. Это так называемый глиоксилатный цикл. Свое наименование этот путь получил по названию промежуточного продукта превращения изоцитрата в оксалоацетат: расщепление изоцитрата дает глиоксилат и сукцинат, а глиоксилат, соединяясь с ацетил-КоА, превращается в малат и далее в оксалоацетат. Эта биохимическая вставка требует присутствия двух особых ферментов. Первый расщепляет изоцитрат, а второй — объединяет сукцинат и глиоксилат. Обладатели этой сопряженной с циклом Кребса вставки могут расти на соединениях уксусной кислоты (на ацетате). Итак, если у организма имеются оба фермента глиоксилатного цикла и он растет, потребляя ацетат, то отсюда следует, что он использует именно глиоксилатный путь синтеза лимонной кислоты.
Биохимическая задачка решалась с двух сторон: экспериментально с последующим тестированием продуктов жизнедеятельности бактерий и с помощью сравнения геномов разных бактерий и архей.
Ученые растили Haloarcula из Мертвого моря на двух средах — ацетатной и сукцинатной. Затем выясняли, какие различия в экспрессии генов были наиболее четкими в двух вариантах. Для ацетатной версии выявились четыре фермента, отсутствующие у сукцинатных бактерий. Гены этих ферментов считываются все вместе и располагаются вблизи других ферментов синтеза ацетил-КоА.
Это означает, что все ферменты увязаны в одну метаболическую операцию, совмещенную с работой ацетил-КоА. Ученые предположили гипотетическую биохимическую цепочку, в которой участвовали бы все эти ферменты. Это оказалось превращение лимонной кислоты в известный уже нам изоцитрат (часть, общая для всех циклов), а затем превращение этого продукта в глутамат (название «глутамат натрия» сейчас всем известно, так как широко используется как вкусовая добавка практически во всех специях и сухих концентратах). Образование глутамата и метиласпартата — ключевые звенья этого метаболического пути — возможно в среде, богатой азотными соединениями (в нашем случае читай — органикой), так как для протекания реакций необходим ион аммония. С помощью методов высокоразрешающей жидкостной хроматографии ученые обнаружили присутствие промежуточных продуктов метиласпартатного пути. Таким образом, гипотетический путь приобрел вполне материальное подтверждение.
Гены ферментов метиласпартатного цикла схожи с генами разных бактерий, а не архей. Это означает, что они были приобретены археями путем горизонтального переноса. При этом у бактерий гомологичные ферменты выполняют совсем другие функции и катализируют вовсе не схожие реакции. Но, видимо, эти ферменты были необходимы (или, лучше сказать, удобны) галофильным археям, потому они приобрели соответствующие гены, преобразовали их и скомпоновали в оперон для выполнения новых, специфических функций.
Почему метиласпартатный цикл мог оказаться полезным для архебактерий? Ведь если судить попросту, то бактерии должны получить из изоцитрата глиоксилат и сукцинат. Те, кто использует глиоксилатный путь, проделывают эту процедуру за два шага, а метиласпартатные изобретатели — за целых девять. Да еще требуется среда, богатая органикой. К чему все эти усложнения? Ученые предположили, что в сверхсоленых условиях накопление глутамата могло принести двойную или даже тройную пользу. Во-первых, реализовать метиласпартатный путь синтеза малата. Во-вторых, поддерживать за счет глутамата осмотическое равновесие с внешней средой. В-третьих, использовать полимеры глутамата в качестве запасных веществ на случай голодания. Два последних преимущества могли стать удачным решением жизненных проблем для галофилов, существующих при неравномерном поступлении органических веществ в водоем.
Эта сложная биохимическая работа замечательно иллюстрирует методы, которыми пользуется население микромира. Если им выгодно (энергетически или материально) использовать тот или иной субстрат, то они могут легко позаимствовать нужный ген или несколько, инкорпорировать их в свой геном, подправить для выполнения новых функций, соединить с другими — и вот уже прежде враждебная среда становится удобной и обжитой.
Подобные исследования должны постепенно убедить нас, что в мире бактерий изоляция геномов отдельных организмов и отдельных видов имеет совсем другие ограничения и, возможно, другую природу, чем в привычном нам макромире.
Наш сайт поможет вам купить квартиру в Костроме от собственника и без лишних посредников.


